Als „Chemisches Pendel“ fand diese Reaktion Eingang in die Chemieolympiade und zwar über die Physikolympiade. So weit, so gut.
Die Sensation an dieser Reaktion ist, dass sich nicht wie bei fast allen Reaktionen ein chemisches Gleichgewicht zwischen Ausgangsstoff und Produkt einstellt, sondern vielmehr mehrere Gleichgewichtsreaktion in einem Zusammenspiel zwischen zwei Zuständen hin und her oszillieren. Diese Tatsache galt lange als unmöglich, da nach dem 2. Hauptsatz der Thermodynamik die Ordnung eines Systems immer nur abnehmen kann. Das gilt allerdings nur für abgeschlossene Systeme und nicht für eine (selbstverständlich nicht ewig) oszillierende Reaktion (die Sauerstoff abgibt).
Vorbereitung
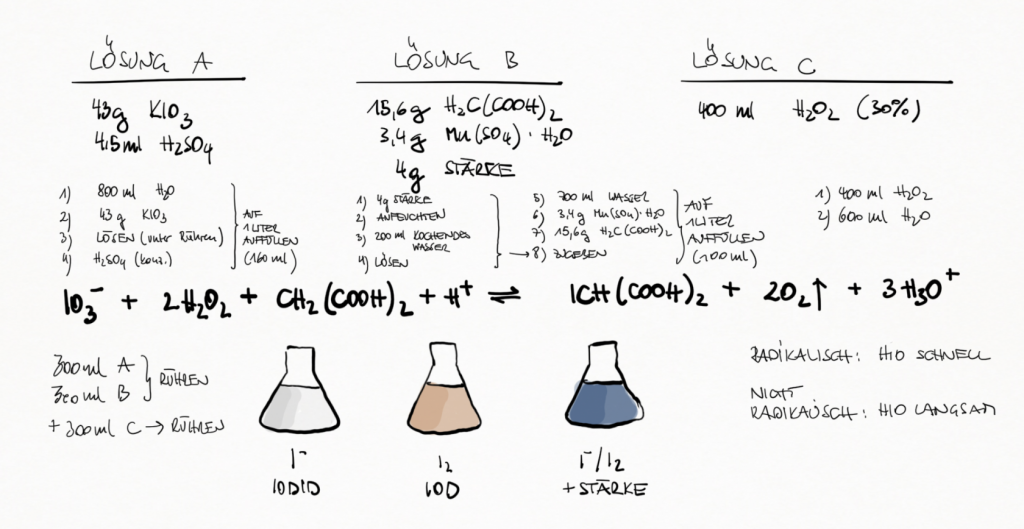
Stelle folgende drei Lösungen A, B und C her.
Lösung A
43 g KIO3
4.5 ml H2SO4
Lösung B
15.6 g H2C(COOH)2
3.4 g Mn(SO4).H2O
4 g Stärke
Lösung C
400 ml H2O2
Anleitung zur Herstellung
Durchführung
Füge zu gleichen Menge von Lösung A und Lösung B unter heftigem Rühren Lösung C (wieder gleiche Menge) hinzu.
Beschreibung
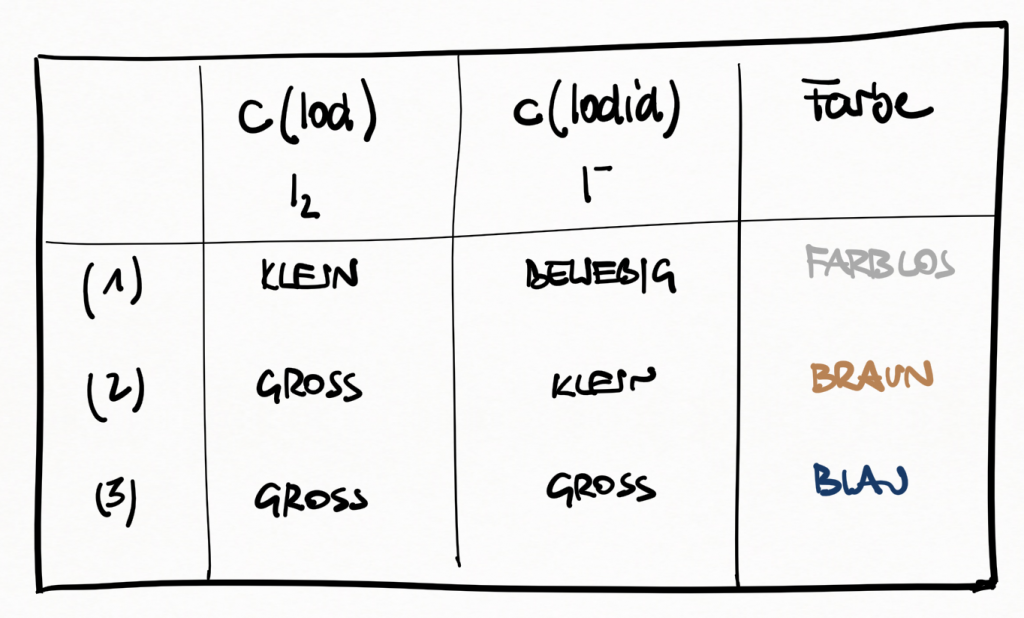
Kaliumiodat reagiert unter Abgabe von Sauerstoff zu Iodid. Das Gleichgewicht geht aber über zahlreiche Zwischenreaktionen Das Ergebnis ist ein wechselndes Farbspiel zwischen farblos, braun und blau.
Das Ergebnis ist ein wechselndes Farbspiel zwischen farblos, braun und blau.