Zuerst einmal muss man Dalton glauben. Materie besteht aus kleinsten Teilchen, die (zwar nicht unteilbar sind aber dennoch) sich zu kleinen Konglomeraten namens Molekülen zusammenschließen.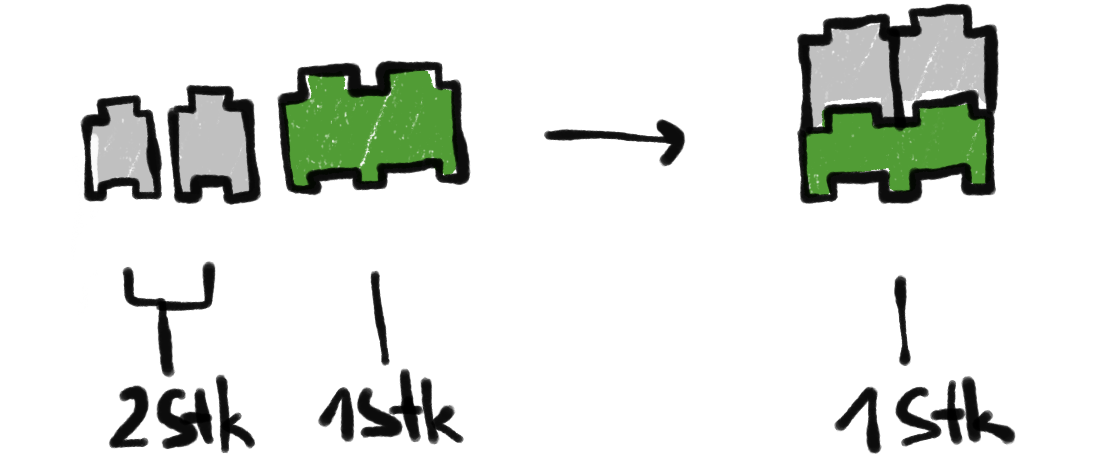 Kein Wort über die Chemische Bindung an dieser Stelle, aber die Zahlenspiele sollen korrekt dargestellt werden.
Kein Wort über die Chemische Bindung an dieser Stelle, aber die Zahlenspiele sollen korrekt dargestellt werden.
Wir verwenden natürlich eine entsprechende Schreibweise und keine Bausteine, die uns nur im Verständnis unterstützen.
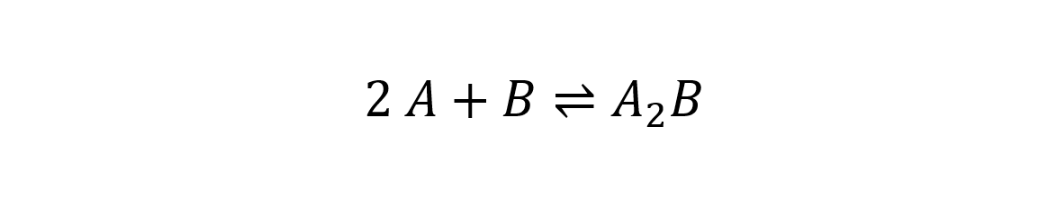 Nun kommen aber die Ausgangsstoffe der chemischen Reaktionen nur in den seltensten Fällen als Einzelbausteine (also atomar) vor. Eine große Rolle spielt das aber in der Systematik nicht.
Nun kommen aber die Ausgangsstoffe der chemischen Reaktionen nur in den seltensten Fällen als Einzelbausteine (also atomar) vor. Eine große Rolle spielt das aber in der Systematik nicht.
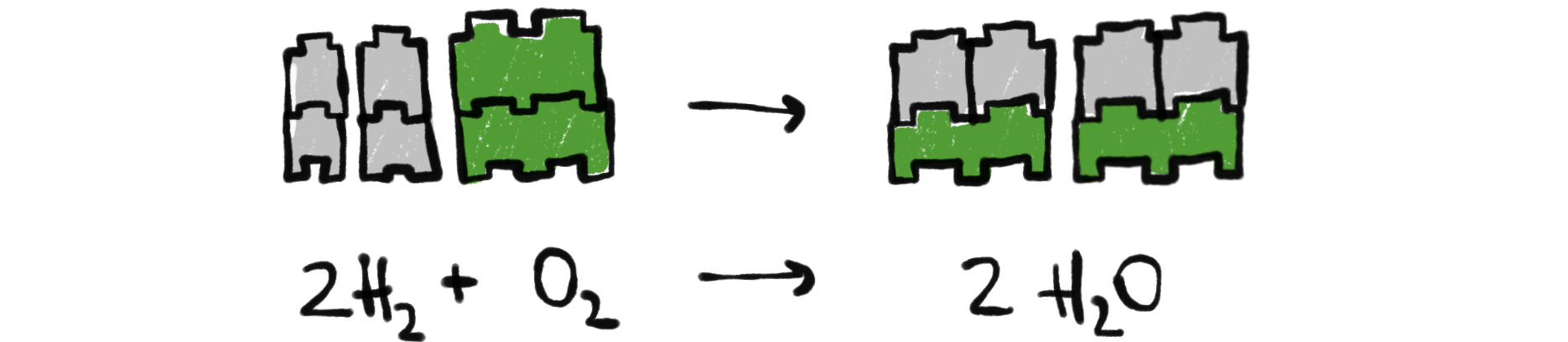 In chemischer Schreibweise also
In chemischer Schreibweise also
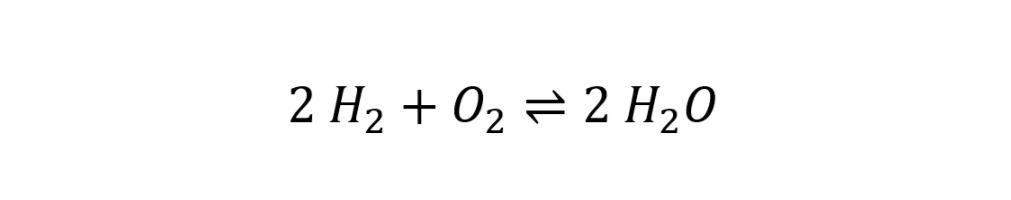 Anpassen der Koeffizienten
Anpassen der Koeffizienten
Die Bausteine an sich können in einer Reaktionsgleichung nicht verändert werden. Um die Bilanz in einer Gleichung richtig zu stellen (also die Anzahl der beteiligten Atome links und rechts auszugleichen) ist es möglich, die Koeffizienten der beteiligten Stoffe entsprechend anzupassen.
Beispiel: Verbrennung von Benzen
Zuerst werden die beteiligten (unveränderbaren) Ausgangsstoffe und die resultierenden Produkte angeschrieben.
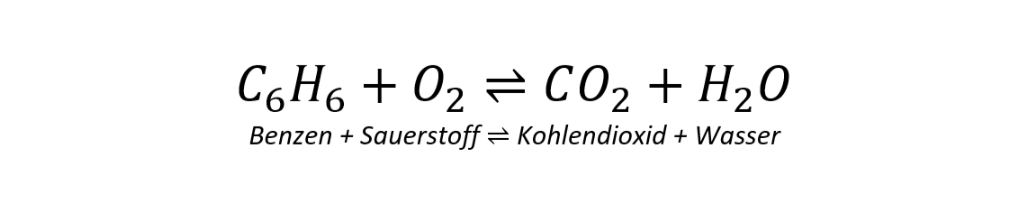 Erst im zweiten Schritt werden nun die Koeffizienten so angepasst, dass die Summe der Atome auf der linken Seite gleich der Summe der Atome auf der rechten Seite ist.
Erst im zweiten Schritt werden nun die Koeffizienten so angepasst, dass die Summe der Atome auf der linken Seite gleich der Summe der Atome auf der rechten Seite ist.
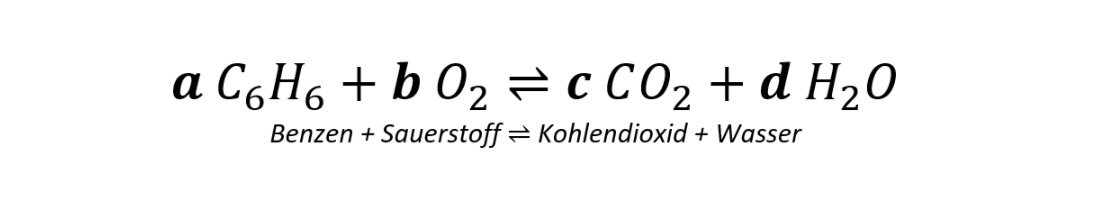
Möglichkeit 1 – Sinnvolles Probieren
Man beginnt mit einem Koeffizienten eines Atoms, das links und rechts jeweils in genau einer Verbindung vorkommt. Möglich ist das hier mit C oder H. Hier wird der Koeffizient zuerst angepasst. Es wird von links nach rechts gearbeitet
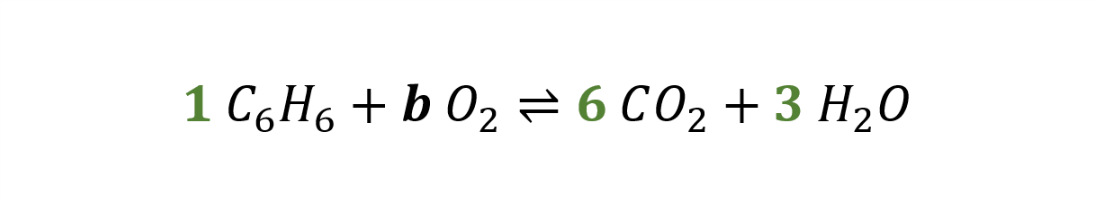 Nun von rechts nach links. Angepasst wird hier noch der Sauerstoff.
Nun von rechts nach links. Angepasst wird hier noch der Sauerstoff. 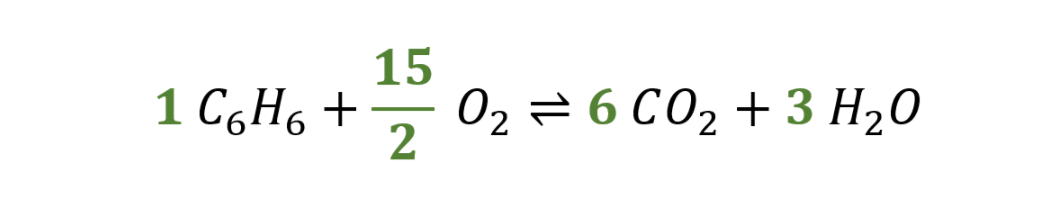 Zuletzt mag man keine Brüche als Koeffizienten, man ermittelt die kleinesten ganzzahligen, indem man mit dem entsprechenden Faktor (hier 2) multipliziert.
Zuletzt mag man keine Brüche als Koeffizienten, man ermittelt die kleinesten ganzzahligen, indem man mit dem entsprechenden Faktor (hier 2) multipliziert.
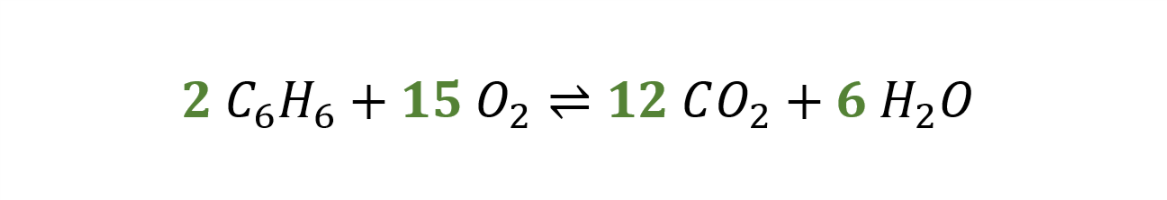 Möglichkeit 2 – Mit Gleichungen berechnen
Möglichkeit 2 – Mit Gleichungen berechnen
Aus den mit Variablen ausgedrückten Koeffizienten lässt sich für jedes Element die Bilanzgleichung aufstellen. Die Summe der Atome eines Elements auf der linken Seite gleicht der Summe der Atome eines Elements auf der rechten Seite.
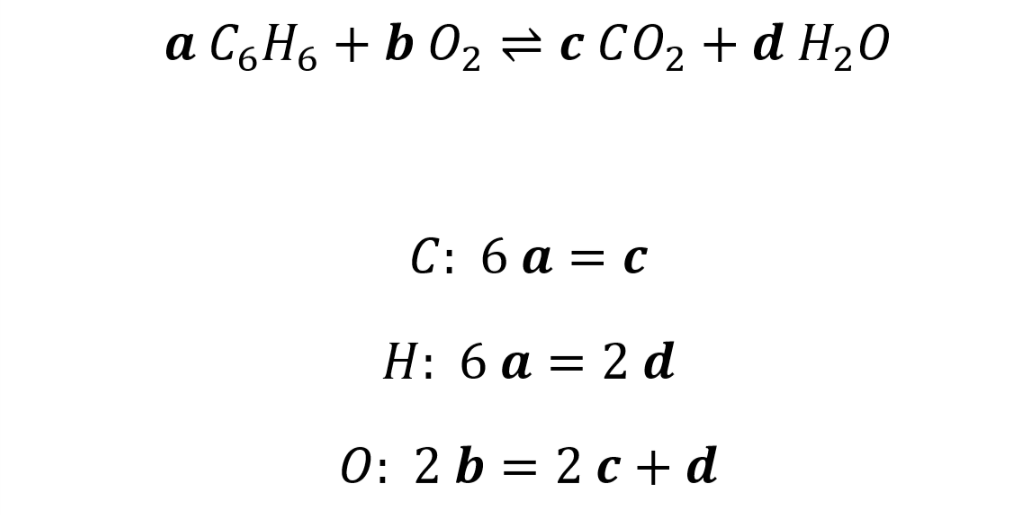 Es handelt sich hierbei um drei Gleichungen für vier Unbekannte. Mathematisch also nicht ausreichend bestimmt, um eine eindeutige Lösung zu erhalten. Das ist aber selbstverständlich, da die Lösung des Gleichungssystems ja niemals eindeutig ist, Vielfache einer Lösungsmöglichkeit müssen selbstverständlich ebenfalls Lösungen des Gleichungssystems sein.
Es handelt sich hierbei um drei Gleichungen für vier Unbekannte. Mathematisch also nicht ausreichend bestimmt, um eine eindeutige Lösung zu erhalten. Das ist aber selbstverständlich, da die Lösung des Gleichungssystems ja niemals eindeutig ist, Vielfache einer Lösungsmöglichkeit müssen selbstverständlich ebenfalls Lösungen des Gleichungssystems sein.
Lösen lässt sich dieses Gleichungssystem wie gewohnt (Substitution, Eliminerung, …)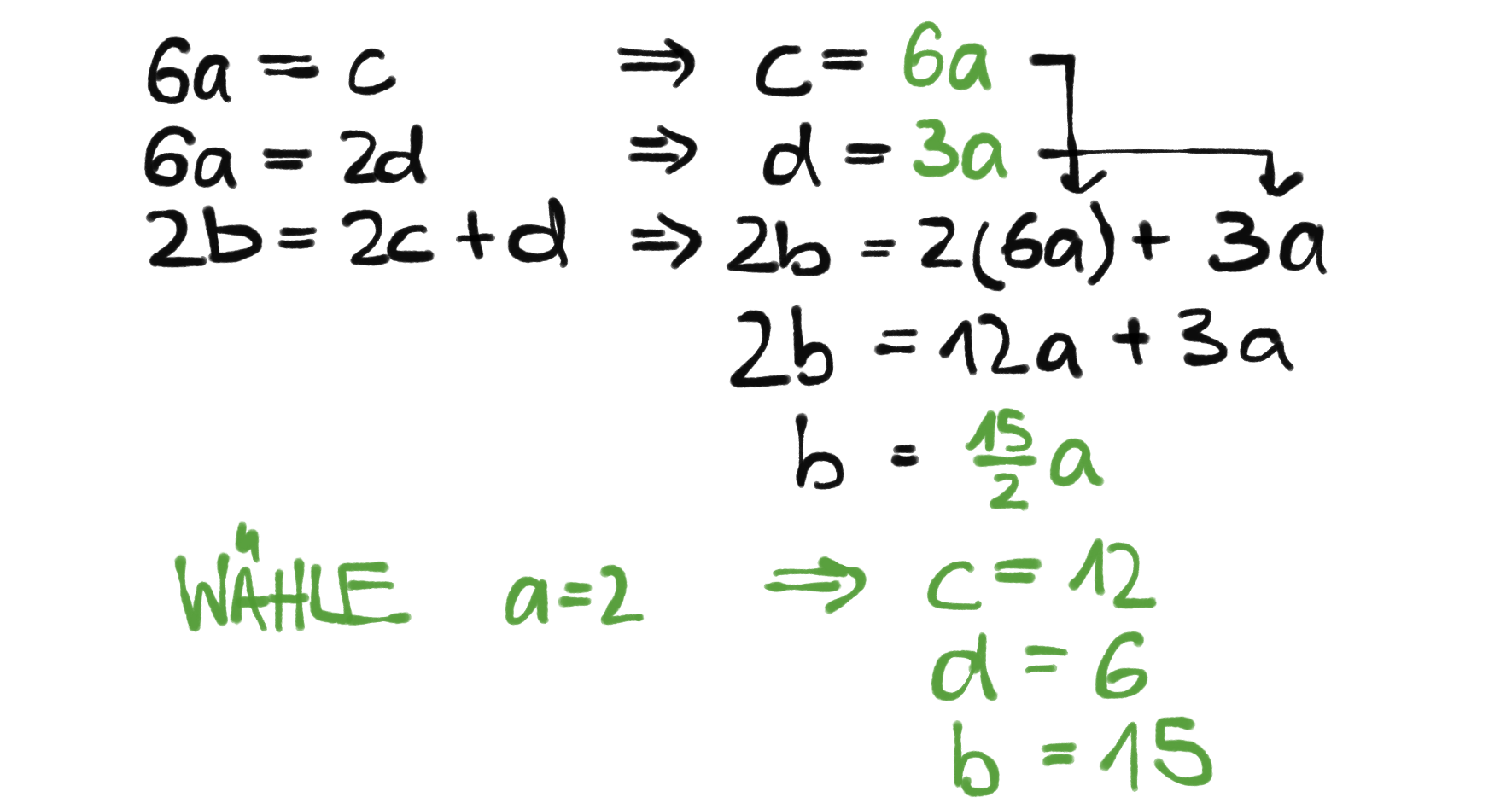 Und damit auch hier also das selbe Ergebnis. Nur ohne Probieren.
Und damit auch hier also das selbe Ergebnis. Nur ohne Probieren.
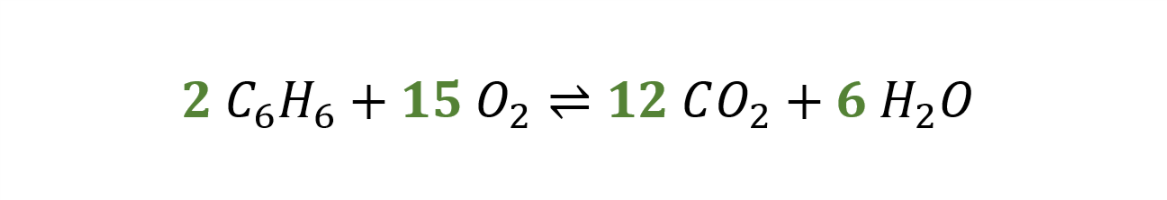 Weitere Beispiele
Weitere Beispiele
Stimme folgende Reaktionsgleichungen ab
(1) Al + Cl2 → AlCl3
(2) C3H8 → C2 + H2O
(3) Na + O2 → Na2O
(4) Mg + I2 → MgI2
(5) CuO + Fe → FeO + Cu
(6) C8H18 + O2 → CO2 + H2O
(7) C5H10 + O2 → CO2 + H2O
(8) C7H16 + O2 → CO2 + H2O
(9) C2H6O + O2 → CO2 + H2O
(10) FeS2 + O2 → Fe2O3 + SO2
Schreibe folgende Reaktionsgleichungen an
(1) Bildung von Eisen(III)-oxid aus den Elementen
(2) Verbrennung (=Reaktion mit Sauerstoff) von Aluminium
(3) Kupfer(II)-oxid reagiert mit Wasserstoff zu einem Metall und einer bekannten Molekülverbindung
(4) Magnesium reagiert mit Salzsäure zu einem Salz und einem brennbaren Gas
(5) Natrium reagiert mit Wasser
(6) Schwefeldioxid reagiert mit Sauerstoff zu Schwefeltrioxid
(7) Zerlegung von Wasser in die Elemente
Beachte – Bei einer chemischen Reaktion müssen auch die Ladungen vor und nach der Reaktion übereinstimmen.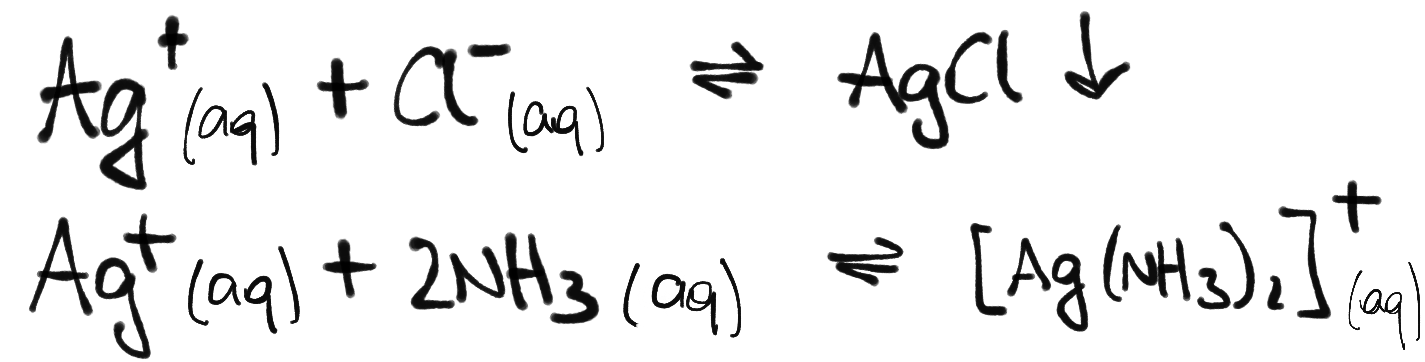 Stimme die folgenden Reaktionsgleichungen ab
Stimme die folgenden Reaktionsgleichungen ab
(1) Ba3N2 + H2O → Ba(OH)2 + NH3
(2) Cu + NO3– + H+ → Cu2+ + NO + H2
(3) Cr2O72- + H2O + H+ → Cr3+ + S + H2O